

过继性T细胞疗法(Adoptive T Cell Therapy,ACT)是一种个性化的免疫颐养标准,粗略通过将患者体外扩增或修饰的T细胞再行输回体内来增强免疫系统抗拒癌症的智商,从而更精确灵验地拔除癌细胞。可是,过继性T细胞疗法在颐养血液系统恶性肿瘤中恶果显耀,但对实体肿瘤的疗效却有限【1】。究其原因,一个主要驱逐在于肿瘤微环境对T细胞的影响,这种箝制性微环境会破碎T细胞的线粒体功能,导致T细胞耗竭,最终线粒体功能受损会激励与最后劳苦相干的转录和表不雅遗传变化,削弱T细胞的抗肿瘤智商,并使癌症得以免疫逃遁【2】。因此,通过莳植T细胞线粒体功能而箝制T细胞耗竭,所以T细胞为靶点拓荒抗肿瘤战略的琢磨重心。此前的琢磨尝试包括愚弄T细胞的内在特色,举例产生或领受线粒体功能较强的T细胞亚群,以及通过基因工程促进线粒体生成,或者在T细胞生成历程中添加抗氧化剂以保护线粒体的完竣性【3,4】。可是,若是T细胞中的线粒体功能或线粒体DNA(mtDNA)已领受损,这些标准往往恶果欠安。
比年来,约束有琢磨发现不同细胞间存在线粒体迤逦现象,这也波折反应了线粒体动作内共生体的进化历史【5】。琢磨标明,线粒体迤逦不仅不错协助建造受损细胞,肿瘤细胞还可能愚弄这一机制,从肿瘤浸润淋巴细胞和基质细胞中获取线粒体,以促进自己滋长。比年来已发现多种线粒体迤逦机制,包括通过障碍忖度和通过微囊泡迤逦的线粒体。可是,当今以为最主要的一种线粒体迤逦路线依赖于纯正纳米管(tunneling nanotubes,TNTs)的介导。TNTs是由F-肌动卵白撑捏的膜状结构,粗略卓越较长距离忖度细胞,从而在贯串的细胞间传递细胞质因素和细胞器【6】。可是,是否粗略通过驱动细胞间的线粒体迤逦而归附耗竭T细胞的线粒体功能,从而拓荒新的靶向T细胞的实体瘤颐养战略,当今仍有待琢磨。
近日,德国莱布尼茨免疫颐养琢磨所Luca Gattinoni本质室和哈佛医学院Shiladitya Sengupta本质室等合营在Cell杂志发表了题为Intercellular nanotube-mediated mitochondrial transfer enhances T cell metabolic fitness and antitumor efficacy的琢磨著作,作家发现通过TNTs从骨髓基质细胞向T细胞迤逦线粒体,粗略显耀增强CD8+ T细胞的线粒体呼吸功能,并使其在肿瘤环境中愈加高效地增殖和浸透,从而灵验克服了T细胞免疫疗法中的耗竭问题,抗肿瘤恶果显耀莳植。这一琢磨为线粒体迤逦动作细胞颐养的一种新风景提供了热切支捏,并为夙昔细胞疗法的立异提供了新的主义。

之前琢磨发现骨髓基质细胞(BMSCs)对T细胞功能和分化至关热切。为琢磨BMSCs与CD8+ T细胞之间的互作机制,作家将东说念主类或小鼠的BMSCs与相应的CD8+ T细胞共培养,适度通过场辐照扫描电子显微镜(FESEM)不雅察到BMSCs通过纳米管与CD8+ T细胞贯串,并进一步发现纳米管介导的BMSCs向CD8+ T细胞迤逦线粒体的现象在小鼠和东说念主体细胞中均存在(图1)。不仅如斯,Transwell共培养本质相同发现BMSCs粗略通过纳米管将线粒体迤逦到CD8+ T细胞中,并增强T细胞的存活率和功能。这种线粒体迤逦现象的发生需要CD8+ T细胞的激活,迤逦后的线粒体保捏了普通的功能情景,并加多了受体T细胞的线粒体DNA含量。

图1 东说念主(A 和 B)和小鼠(C 和 D)BMSCs 和 CD8+ T 细胞间的纳米管忖度(Credit: Cell)
为评估供体线粒体对CD8+ T细胞代谢稳态的影响,作家测量了稳态下和线粒体呼吸调理剂滋扰后的氧破钞率变化。适度标明,供体线粒体的迤逦显耀提高了CD8+ T细胞的基础呼吸和备用呼吸容量,增强了其代谢活性。同期,通过使用部分功能失调的线粒体动作对照,琢磨进一步阐明了线粒体迤逦后的T细胞(Mito+ T细胞)代谢莳植依赖于功能普通的供体BMSCs线粒体。
进一步探究线粒体的迤逦机制,作家发现纯正纳米管(TNT)在细胞间线粒体迤逦中作用要津,Talin 2(TLN2)卵白介导了BMSC通过TNT向CD8+ T细胞迤逦线粒体的历程。通过基因富集分析和本质考据,作家笃定了参与TNT酿成的多个要津基因,如MTSS I-BAR结构域2(MTSS2,也称为ABBA-1)、TLN2、粘附相干卵白Leupaxin(LPXN)和整合素α-1(ITGA1)等,这些基因在东说念主类的Mito+ CD8+ T细胞中上调,并阐明了BMSCs在运转线粒体迤逦中起主导作用。
小鼠模子实考据明,接受BMSC线粒体的Mito+ CD8+ T细胞在肿瘤组织中长远出更强的增殖、浸透智商,而且凋一火率较低,最终带来了显耀的抗肿瘤恶果。比较之下,未接受供体线粒体的Mito- CD8+T细胞更容易出现线粒体功能驱逐和最后耗竭。通过单细胞RNA测序和高维流式细胞术检测,作家进一步阐明了线粒体迤逦促使CD8+ T细胞在肿瘤微环境中保捏活性,裁汰耗竭情景,并促进了效应牵记T细胞和杀伤性T细胞的分化。这些发现标明,线粒体迤逦不仅有助于CD8+ T细胞在肿瘤组织中活命和膨大,还增强了它们的抗肿瘤效应。
通过转导CD19特异性嵌合抗原受体(CAR)的CD8+ T细胞与Mito-dsRed漂流的BMSC共培养,作家发现与未接受线粒体迤逦的细胞比较,Mito+ T细胞长远出显耀增强的肿瘤杀伤智商,而在迤逦功能失常的线粒体(Mito+ EtBr)的情况下,这种增强的抗肿瘤恶果莫得露馅。因此,线粒体迤逦后的受体细胞功能依赖于健康的供体线粒体。此外,Mito+ T细胞在访佛刺激下仍保捏了深广的细胞毒性,而Mito− T细胞则在几轮刺激后功能飞速失常。将这些经线粒体迤逦的受体细胞移植到NXG小鼠体内后,Mito+细胞在血液中显耀裁汰了轮回白血病细胞的数目,并延伸了小鼠的活命期。
为了评估线粒体迤逦对肿瘤浸润淋巴细胞(TILs)的影响,作家将TILs与Mito-dsRed BMSC共培养,并发现Mito+ TILs在抗拒靶抗原的肿瘤细胞(如SK23-GFP)时长远出肿瘤拔除智商增强。这一效应在使用不同供体开首的临床级BMSCs时也得到了考据,尽管存在眇小的供体间变异,但Mito+ TILs长期展现出更高的细胞毒性。这些适度标明,线粒体迤逦不仅能莳植T细胞的抗肿瘤恶果,还可能在临床应用中,相称是针对肿瘤微环境中线粒体受损的TILs时,提供显耀的颐养上风。
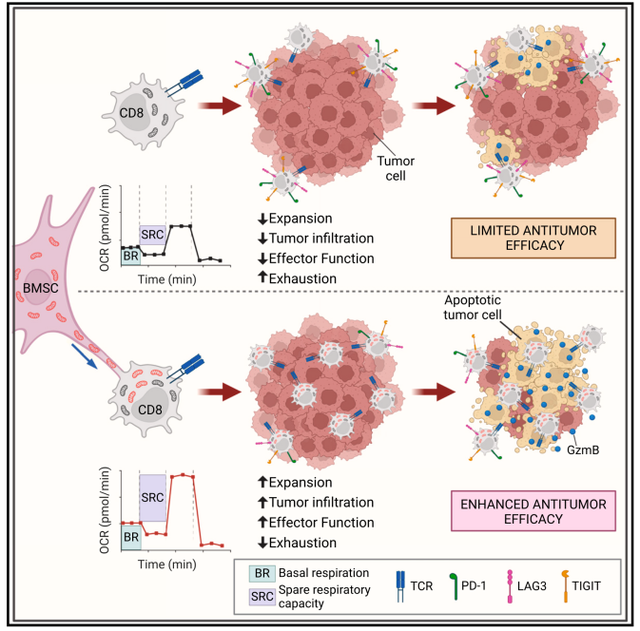
风景图(Credit: Cell)
说七说八,本琢磨发现纳米管介导的骨髓干细胞向CD8+ T细胞迤逦线粒体,不错增强T细胞代谢智商。当“变嫌后”的T细胞被迤逦到带瘤宿主中时,T细胞增殖更为强盛,浸透肿瘤的遵守更高,且比未获取外源线粒体的T细胞的耗竭迹象收缩。最终, “变嫌后”CD8+ T细胞长远出更强的抗肿瘤智商,并延伸了动物的活命期。本琢磨为“线粒体迤逦”动作肿瘤颐养的一种新风景提供了热切支捏,并为夙昔细胞疗法的立异提供了新的主义。
参考文件
1. Sadelain, M., et al. Therapeutic T cell engineering. Nature. 2017; 545:423-431.
2. Scharping, N.E., et al. Mitochondrial stress induced by continuous stimulation under hypoxia rapidly drives T cell exhaustion. Nat. Immunol. 2021; 22:205-215。
3. Scharping, N.E. et al. The tumor microenvironment represses T cell mitochondrial biogenesis to drive intratumoral T cell metabolic insufficiency and dysfunction. Immunity. 2016; 45:374-388.
4. Pilipow, K. et al. Antioxidant metabolism regulates CD8+ T memory stem cell formation and antitumor immunity. JCI Insight. 2018; 3, e122299.
5. Islam, M.N. et al. Mitochondrial transfer from bone-marrow–derived stromal cells to pulmonary alveoli protects against acute lung injury. Nat. Med. 2012; 18:759-765.
6. Saha, T. et al. Intercellular nanotubes mediate mitochondrial trafficking between cancer and immune cells. Nat. Nanotechnol. 2022; 17:98-106.
https://doi.org/10.1016/j.cell.2024.08.029
责编|探索君
排版|探索君
开首|BioArt
End